La enfermedad del cáncer sigue ocupando importantes esfuerzos en los estudios que sobre ella se realizan, sobre sus diversas manifestaciones, especialmente, en lo que se refiere a su existencia y vigencia entre los humanos, pugnando por encontrar caminos de curación y prevención, de este muy antiguo mal que afecta en general a los seres vivos, incluso, en su momento a aquellas especies hoy extintas.
Una célula de cáncer de seno (mama) que se multiplica.
Fuente: Fuente: Instituto Nacional del Cáncer/ Instituto del Cáncer de la Universidad de Pittsburgh
Una revisión sobre esta enfermedad puede comenzar con lo que apunta la Organización Mundial de la Salud (OMS), como su definición: es un término amplio utilizado para aludir a un conjunto de enfermedades que se pueden originar en casi cualquier órgano o tejido del cuerpo cuando células anormales crecen de forma descontrolada, sobrepasan sus límites habituales e invaden partes adyacentes del cuerpo y/o se propagan a otros órganos. Propicia que un grupo de células, que forman parte del organismo, en algún momento, modifican su comportamiento, se colocan fuera del control metabólico, contrariando el funcionamiento normal, y se reproduzcan en forma ilimitada, de forma tal, que se diseminan por el resto del cuerpo del ser afectado, dando lugar a un proceso que es llamado "metástasis".
El cáncer puede iniciar en cualquier parte del cuerpo, para el caso de los humano formado por alrededor de treinta billones de células. En condiciones de un organismo sano, las células humanas se forman y se multiplican (mediante un proceso que se llama división celular) para formar células nuevas a medida que el cuerpo las necesita. Cuando las células envejecen o se dañan, mueren y las células nuevas las reemplazan. Excepcionalmente no sigue este orden y las células anormales o células dañadas se forman y se multiplican cuando no deberían. Estas células, fuera de control, es muy posible que se aglutinen y formen tumores, que son bultos de tejido, es decir malformaciones. Dichos tumores se clasifican en: cancerosos (denominados malignos) o no cancerosos (nombrados benignos).
Estas malformaciones malignas se diseminan, buscan invadir los tejidos cercanos. Sin que se conozca a exactitud la razón, no se comportan afectando sólo localmente, entonces alternativamente buscan trasladarse a otras partes del cuerpo y formar nuevos tumores, este es un proceso que se conoce como "metástasis". De acuerdo al órgano primordialmente afectado se le tipifica. La mayoría de los tipos de cáncer forman tumores sólidos. Pero cuando la variedad del cáncer afecta el tejido sanguíneo, en general, no se forman tumores sólidos.
Los tumores benignos, tienen comportamientos que se sujetan al control del organismo, por ejemplo: ni se diseminan a los tejidos cercanos, ni tampoco hacen "metástasis"; al extirparlos no suelen volver, sin embargo, estos tumores en ocasiones son bastante grandes y como consecuencia de su volumen, podrían llegar a causar síntomas graves o poner en peligro la vida de la persona, como acontece cuando los tumores benignos se sitúan en el cerebro o el encéfalo.
Por otra parte, los tumores cancerosos a veces, después de ser removidos, vuelven. Son entes indisciplinados, presentan comportamientos anormales, lo que atenta contra el funcionamiento del organismo, sus acciones son, entre otras, lograr que los vasos sanguíneos crezcan de tal manera que apoyen su sobrevivencia, pues dichos vasos sanguíneos, se encargan de aprovisionarlos con oxígeno y nutrientes, e incluso retiran los productos de desecho que ellos generan. Por otra parte se "disfrazan" químicamente y se esconden del sistema inmunitario, anulando la función de este sistema, cuya tarea es la de destruir esas células anormales.
Se sabe que las células afectadas con el cáncer, modifican su contenido genético, alterando el contenido de sus cromosomas, llegando a poseer el doble de cromosomas que normalmente debieran de tener, dichas células dependen de nutrientes que son distintos a los que necesitan las células normales y algunas crean energía de los nutrientes de formas diferentes a las que usan las células normales, lo que propicia que se reproduzcan desordenadamente, mucho más rápido.
Por lo anterior se establece que el cáncer es una enfermedad genética, los cambios que se producen en el comportamiento de las células afectadas, son el "modus operandi" de la enfermedad. En general, el cuerpo elimina células con daños en el "ácido desoxirribonucleico" (ADN) antes de que se vuelvan cancerosas. Pero hay distintos factores que ocasionan que la capacidad del organismo disminuya, como es el envejecimiento. Por eso el riesgo de cáncer aumenta con la edad.
Se ha podido observar que el cáncer en cada persona es una combinación única de cambios genéticos. A medida que el cáncer sigue creciendo, ocurren otros cambios. Incluso dentro del mismo tumor, es posible que las diversas células tengan cambios genéticos diferentes. Se puede concluir que a cada ser vivo le atañen causas distintas que pueden incidir en el surgimiento de la enfermedad, mutaciones, por factores internos, como pueden ser alteraciones de carácter aleatorio en el momento de la reproducción celular, o bien por factores externos, por la incidencia de sustancias perjudiciales en el medio ambiente, como son las sustancias químicas, por ejemplo, las contenidas en el humo del tabaco o los rayos ultravioletas del sol. O bien por herencia de los antecesores, contenida en los mismos genes que se propiciaron en la gestación.
A la fecha se tienen establecidos más de cien tipos de cáncer. En general, los tipos de cáncer llevan el nombre de los órganos o tejidos donde se forma inicialmente el cáncer. Por ejemplo, el cáncer de pulmón se inicia en el pulmón, y el cáncer de encéfalo se inicia en el encéfalo. A veces el cáncer se describe por el tipo de células que lo formaron, como las células epiteliales o las células escamosas.
El cáncer metastásico tiene el mismo nombre y el mismo tipo de células cancerosas que el cáncer primario. Por ejemplo, el cáncer de seno (mama) que forma un tumor metastásico en el pulmón es cáncer de seno metastásico, no es cáncer de pulmón.
Cuando se observan al microscopio, las células cancerosas metastásicas en general se ven igual que las células del cáncer primario. Es más, las células cancerosas metastásicas y las células del cáncer primario suelen tener características moleculares en común, como cambios específicos en los cromosomas.
En algunos casos, el tratamiento ayuda a prolongar la vida de las personas con cáncer metastásico. En otros casos, la meta principal del tratamiento del cáncer metastásico es evitar que se disemine o aliviar los síntomas de la enfermedad. Los tumores metastásicos la mayor parte de la ocasiones causan daños graves que afectan el funcionamiento del cuerpo. La "metástasis" causa la mayoría de las muertes por cáncer.
El avance obtenido a la fecha sobre esta enfermedad indica que existen tres tipos de afectación genética: "Proto-oncogen", "Gen Supresor Tumoral"" y "Gen de reparación del "ácido desoxirribonucleico" (ADN).
Los primeros Proto-oncogen, participan en la formación y multiplicación normal de las células. Hay circunstancias que implican, cuando hay ciertos cambios en estos genes o hay más actividad de la normal, que pueden transformarlos en genes que causen cáncer, se les conoce como "oncogenes". Esto propicia que las células se multipliquen y sobrevivan en casos en los que normalmente no deberían.
Los genes supresores tumorales también controlan la formación y multiplicación de las células, entonces resulta que las células con ciertos cambios en los genes supresores tumorales podrían entrar a una fase incontrolada de reproducción.
Por último, en el caso de los genes de reparación de ADN, que corrigen el ADN dañado. Las células que presentan mutaciones en estos genes tienden a presentar más mutaciones en otros genes y cambios en los cromosomas (como trozos de cromosoma repetidos o faltantes). Cuando coinciden ambos tipos de mutaciones, es posible que las células se vuelvan cancerosas.
En la medida que los avances en los conceptos médicos aplicables, normalmente generados por la aplicación de nuevas tecnologías, se ha vuelto de mayor alcance el conocimiento de las circunstancias que viven las células componentes del organismo, es por ello que ahora se pueda dar seguimiento a los cambios moleculares que propician el surgimiento de la enfermedad.
En estos tiempos, y desde hace algunos años, se conoce que hay cierto tipo de mutaciones que se tornan incidentes para algún tipo de cáncer específico, por lo que se aprovecha esta información para diagnosticar con antelación el padecimiento y prescribir tratamientos específicos.
Las células normales, con el transcurso del tiempo, a veces se convierten cancerosas. Antes de que las células cancerosas se formen en los tejidos del cuerpo, suelen sufrir cambios anormales que se llaman "hiperplasia" y "displasia" respectivamente:
En la "hiperplasia", hay un aumento en el número de células en un órgano o tejido, que se ve normal al microscopio.
Mientras que en la "displasia", las células se ven anormales al microscopio pero no son cancerosas.
Al presentarse estos estados ocurre ocasionalmente, pero no siempre, que la situación se torne en cáncer.
En la actualidad se ha dado un gran paso en la difusión de la información referente a este mal, afortunadamente el nivel de evolución logrado en los estudios sobre el cáncer, permite que en la red existan numerosas hojas que brindan contenido muy valioso, como lo es la hoja del "Instituto Nacional del Cáncer de las Instituciones Nacionales de Salud de Estados Unidos de Norteamérica", de cuyo contenido se ha extraído parte de la información antes expuesta.
Al igual que en los animales, en las plantas también puede ocurrir este tipo de enfermedad, un fenómeno alterativo del desarrollo de la planta. Sin embargo, a diferencia del cáncer animal, en las plantas estos tumores, casi nunca matan a la planta y son respuestas de protección de las plantas al ataque de algún organismo, entre los que destacan los virus, las bacterias, los insectos, los hongos, algunos gusanos y ácaros; pero los más observados, por sus características son los insectos. Estos provocan un crecimiento desmesurado de algún tejido vegetal formando aglomeraciones de células o también conocidos como "agallas".
"Rhizobium radiobacter" . Tomada de Ecured.
En el panorama microscópico, se tiene a la bacteria Agrobacterium, la cual ha sido conocida como un "fitopatógeno" capaz de ocasionar la aparición de agallas y tumores, e inclusive la muerte de las plantas infectadas, principalmente en especies dicotiledóneas y algunas gimnospermas. Ahora bien, Agrobacterium tumefaciens, actualmente conocida como "Rhizobium radiobacter", se sabe bien que es una bacteria que causa en las plantas dicotiledóneas unos tumores conocidos como "agallas" o "tumores del cuello", que crecen en la zona donde se unen la raíz y el tallo.
Los estudios iniciales indicaron que los tumores presentaban alteraciones en el metabolismo de sus "fitorreguladores" y sintetizaban unas sustancias llamadas "opinas", compuestos que las bacterias utilizaban como fuente de carbono y nitrógeno. Estas bacterias, además de su cromosoma circular, poseen material genético extracromosomal de forma circular con un tamaño de aproximadamente 200 kilobases, el cual, por ser responsable de los efectos oncogénicos, ha sido llamado plásmido "Tumor In-ducing" (Ti) "inductor de tumores" o "Root Inducing" (Ri) "inductor de raíces", según si pertenece a una de las dos componentes de la familia Rhyzobiaceae, esto es: Agrobacterium tumefaciens o Agrobacterium rhizogenes, respectivamente. Análisis más detallados mostraron la existencia de un proceso de transferencia de la bacteria hacia las células vegetales de una secuencia de "ácido desoxirribonucleico" ADN llamada "Transferred DNA" (T-ADN) "ADN transferido" presente en el plásmido que poseen.
El Insituto de Ecología A. C. (INECOL) del gobierno federal, por medio de Armando Aguirre-Jaimes y Betsabé Ruíz-Guerra, nos otorga en un muy completo articulo la siguiente información.
Agalla en el tallo de un encino producida por una avispa (Cynipidae, Andricus quercuscalifornicus) (Fotografía obtenida de Naturalista). Tomada de Instituto de Ecología A. C. (Inecol)
El mecanismo de formación de agallas es complejo y es inducido por hormonas del crecimiento vegetal. En el caso particular de los "insectos agalleros", el mecanismo de la formación de agallas comienza cuando el insecto hace una pequeña perforación en algún tejido vegetal para colocar sus huevos; por ejemplo, en las hojas o tallos. Esta acción desencadena el incremento de hormonas que estimulan el crecimiento de los tejidos de la planta, los cuales cubren y aíslan al huevo del insecto. Cuando las larvas emergen se alimentan de estos tejidos, por lo que las agallas proporcionan refugio, alimento, y protección ante las condiciones ambientales y depredadores.
Agallas producidas en una hoja de encino por una pequeña avispa (Cynipidae, Andricus gigas) (Fotografía obtenida de Naturalista). Tomada de Instituto de Ecología A. C. (Inecol)
Las resultantes agallas producidas por los insectos en las plantas, pueden adoptar formas y colores muy diversos, y aún presentarse prácticamente en cualquier parte de la planta, como lo son los tallos, las hojas, las flores, los frutos e inclusive hasta en las raíces. Se sabe que existen alrededor de trece mil especies de insectos formadores de agallas, que abarcan especies de mariposas, escarabajos y pulgones, pero moscas y avispas son los principales grupos de insectos formadores de agallas. Cabe mencionar que cada especie de insecto provoca un tipo específico de agalla, por lo cual es relativamente fácil de reconocer el tipo de insecto formador de agalla. Un ejemplo muy común de insectos formadores de agallas son las avispas, que ovipositan en las hojas de los encinos, las cuales se asemejan una manzana, de color café o rojizo, pero que no pesa y regularmente tiene una hoja pegada tal cual se muestra en la primera fotografía. Otros ejemplos de agallas que podemos identificar fácilmente son aquellas que crecen en las hojas de aguacate, estas protuberancias son producidas por un insecto pequeñito llamado psilido que en su etapa adulta succiona la savia de las plantas.
Corte transversal de un higo (Ficus petiolaris) en el cual se aprecian las avispas (Pegoscapus sp.) emergiendo de una agalla (Fotografía: Eva. M. Piedra-Malagón).
Un ejemplo sorprendente lo constituyen las higueras y sus correspondientes "avispas polinizadoras". Para estas plantas, existen unas diminutas avispas, que entran al higo y depositan sus huevos en las flores, las cuales posteriormente se transformarán en agallas, todo esto se lleva a cabo dentro del fruto. Dichas agallas brindan alimento y seguridad para el desarrollo de las larvas de las avispas, mientras que, el beneficio para la planta consiste en que la otra porción de las flores es polinizada y producirá semillas para hacer viable la conservación de la especie.
Agallas y frutos sanos (vainas) de una leguminosa (Parkinsonia praecox) en el Valle de Tehuacán-Cuicatlán (Fotografía: Armando Aguirre-Jaimes) Tomada de Inecol.
Las investigaciones sobre el particular han determinado que estos tumores muy pocas veces matan a la planta, pero si tienen consecuencias negativas para su desarrollo, a consecuencia de que afectan a las hojas de planta, y con ello entorpecen la realización normal de la fotosíntesis. Adicionalmente, se altera a la planta, en el sentido de que se disminuyen los nutrientes que la planta reserva para su crecimiento, debido a que son tomados por la agalla. Se ha podido observar que algunas especies de insectos inductores de agallas tienen preferencias por las estructuras reproductivas de las plantas, como son las flores o inflorescencias, en estos casos las flores en lugar de producir un fruto y semillas, forma una agalla, lo que afecta negativamente su desarrollo e incluso su reproducción.
Las agallas alcanzan diversas funciones en los ecosistemas, debido a que en adición al propiciamiento del desarrollo de las larvas de los insectos, pueden funcionar también como refugio para otros insectos, una vez que las larvas de los insectos agalleros las abandonan. Por ejemplo, tenemos varias especies de arañas que las utilizan como escondite en espera de capturar presas, también se sabe que diversas especies de hormigas las usan para protegerse de sus depredadores. Los humanos las utilizan con fines farmacológicos, para el tratamiento de infecciones bucales, para combatir diarrea y curar hemorroides. Finalmente se pueden citar usos industriales, como: el curtido de pieles y la fabricación de tintes debido a su alta concentración de taninos, que son compuestos químicos responsables del color rojo. En algunas regiones en México se utilizan de manera lúdica, ornamental y para consumo humano; mientras que en otras regiones de América del Sur se utilizan como control biológico de plantas plaga.
En lo referente al cáncer en animales, la Machincuepa Cuántica dio la información sobre el descubrimiento del mal en dinosaurios que vivieron hace 77 millones de años, en la publicación del 9 de agosto de 2020, "Comprobado: el cáncer existe desde el Jurásico y persiste, aún en el año covid-19". que informó sobre: Un estudio dirigido por el Museo Real Ontario (MRO) y la Universidad McMaster, en Canadá, llevó al descubrimiento y diagnóstico de cáncer de hueso agresivo, un "osteosarcoma", por primera vez en un dinosaurio, según se publicó en la revista "The Lancet Oncology".
El hueso canceroso es el peroné de un "Centrosaurus apertus", dinosaurio con cuernos que vivió hace entre 76 y 77 millones de años. Hallado en el Parque Provincial de Dinosaurios de Alberta en 1989, se pensó en principio que el extremo malformado del fósil se debía a una fractura curativa.
Un avance en el estudio del cáncer de hígado da pauta a esta publicación, por lo que ahora me referiré al órgano multifuncional, que la evolución ha otorgado a los vertebrados, como una herramienta para el buen funcionamiento del organismo, es la glándula más voluminosa de la anatomía y una de las más importantes en cuanto a la actividad metabólica del organismo. Desempeña funciones únicas y vitales, entre ellos la síntesis de proteínas plasmáticas, función desintoxicante y almacenamiento de vitaminas y glucógeno. Además elimina de la sangre muchas sustancias que pueden resultar nocivas para el organismo, transformándolas en otras inocuas.
Para el reino animal, el hígado, es conocido como "el laboratorio del organismo", es un órgano cuyo magnifico trabajo le mantiene con un adecuado metabolismo, y está siendo revisado con intensidad por la comunidad científica, pues su importancia es manifiesta.
El Hígado es la glándula mayor del cuerpo humano y se ha estimado que realiza más de quinientas funciones distintas. Muchas de estas funciones no están relacionadas directamente con el transporte de los nutrientes, pero si correlaciona los sistemas sanguíneos y digestivo, por decir que tiene que ver con todas las sustancias que llegan al aparato digestivo, también regula la mayoría de los niveles de substancias químicas de la sangre y excreta un producto llamado bilis, que ayuda a degradar las grasas, preparándolas para continuar su digestión y absorción. Toda la sangre que sale del estómago y los intestinos pasa a través del hígado. El hígado procesa esta sangre y degrada los nutrientes y drogas de la sangre en formas más fáciles de usar para el resto del cuerpo. Degrada sustancias nocivas, las cuales se excretan hacia la bilis o la sangre. Los subproductos biliares entran en los intestinos y finalmente se eliminan del cuerpo en forma de heces. Mientras que los subproductos sanguíneos son filtrados por los riñones y se eliminan del cuerpo en la orina.
Durante el desarrollo fetal este órgano aparece en la cuarta semana y concluye su principal gestación alrededor de la doceava semana. Cuando el bebé está creciendo en el vientre de la madre, la placenta elimina la bilirrubina del cuerpo del bebé. La placenta es el órgano que crece durante el embarazo para alimentar al bebé. Después del nacimiento, el hígado del bebé comienza a hacer este trabajo. Puede pasar algún tiempo para que el hígado del bebé sea capaz de hacer esto de manera eficiente. Los bebés que han nacido demasiado temprano (prematuros) son más propensos a presentar ictericia que los bebés a término. La ictericia en recién nacidos sucede cuando un bebé tiene un alto nivel de bilirrubina en la sangre. La bilirrubina es una sustancia amarilla que el cuerpo produce cuando reemplaza los glóbulos rojos viejos. El hígado ayuda a descomponer la sustancia de manera que pueda eliminarse del cuerpo en las heces.
Luego entonces las funciones del hígado, incluyen entre otras, las siguientes consideradas principales: producción de bilis, que ayuda a eliminar los desechos y a descomponer las grasas en el intestino delgado durante la digestión; producción de determinadas proteínas del plasma sanguíneo; producción de colesterol y proteínas específicas para el transporte de grasas a través del cuerpo; conversión del exceso de glucosa en glucógeno de almacenamiento , el cual que luego puede ser reconvertido nuevamente en glucosa, para la obtención de energía; regulación de los niveles sanguíneos de aminoácidos, que son las unidades formadoras de las proteínas; procesamiento de la hemoglobina para utilizar su contenido de hierro, pues el hígado almacena hierro; la conversión del amoníaco tóxico en urea, la urea es uno de los productos finales del metabolismo proteico y se excreta en la orina, depuración de la sangre de drogas y otras sustancias tóxicas; regulación de la coagulación sanguínea; resistencia a las infecciones mediante la producción de factores de inmunidad y la eliminación de bacterias del torrente sanguíneo.
El hígado esta formado por varios tipos de células, estas son:
Hepatocitos, constituyen alrededor del ochenta por cierto del peso y del sesenta y cinco por ciento de la población celular del tejido hepático. Son células políedricas que pueden poseer uno o dos núcleos esféricos. Presentan un citoplasma acidófilo con cuerpos basófilos, y son muy ricos en órganulos. Adicionalmente este contiene inclusiones de glucógeno y grasa, su "membrana plasmática" presenta un dominio sinusoidal con microvellosidades que mira hacia el "Espacio de Disse" (que es el sitio de intercambio de materiales entre la sangre y estas células) y un dominio lateral que mira hacia el "hepatocito" vecino. Las membranas plasmáticas de dos hepatocitos contiguos delimitan un canalículo donde será secretada la bilis. La presencia de múltiples orgánulos en el hepatocito se relaciona con sus numerosas funciones: síntesis de proteínas, metabolismo de hidratos de carbono, formación de bilis, catabolismo de fármacos y tóxicos y el metabolismo de lípidos, purinas y gluconeogénesis.
Células de Kupffer, macrófagos fijos pertenecientes al sistema fagocítico mononuclear que se encuentran adheridos al "endotelio" (al que actualmente se le considera un órgano, y ya no una barrera, que sintetiza y secreta diversos productos) y que emiten sus prolongaciones hacia el "Espacio de Disse". Estas células eliminan de la circulación sanguínea, mediante la fagocitosis, todo tipo de partículas extrañas, innecesarias o alteradas, incluyendo eritrocitos envejecidos y bacterias. Además actúan como células presentadoras de antígeno y activan la respuesta inmune de los "linfocitos T", que son producidos en la "médula ósea" y madurados en el "timo" y que forman parte del sistema inmunitario adaptativo.
Células Endoteliales, tapizan la luz de los "sinusoides", tienen un citoplasma fenestrado (con poros) a través del cual penetran los componentes de la sangre en dirección hacia la membrana sinusoidal de los hepatocitos. Morfológicamente son planas, están cubriendo toda la superficie interna de los vasos sangüíneos y por ello siempre están en contacto con la sangre, actúan como reguladoras del tráfico celular y molecular desde la sangre hacia el interior de los tejidos. Poseen una estructura altamente diferenciada y especializada con dos tipos de uniones entre células: unas estrechas (tigh) y otras débiles (gap). Están encargadas de sintetizar y liberar sustancias vasoactivas que regulan el tono vascular, la presión sanguínea y el flujo sanguíneo local; así como también sustancias que participan en la coagulación, en la fibrinolisis y en reacciones inflamatorias e inmunológicas.
Células hepáticas estrelladas o de Ito, presentan una forma de estrella y poseen la capacidad de almacenar lípidos y vitamina A, constituyendo la principal reserva de esta vitamina del organismo. Tras un daño hepático, estas células, que son las principales responsables del proceso fibrogénico, son activadas adquiriendo propiedades contráctiles, proliferativas y profibrogénicas. Durante el proceso de cicatrización, estas células producen una gran cantidad de proteínas de la matriz extracelular, principalmente "colágeno de tipo I". Fueron descubiertas por Toshio Ito (1904 - 1991) en 1956.
Células de Pit, son linfoides residentes en el hígado similares a las células "Natural Killer" (NK) "célula asesina", que es un linfocito del "Sistema Inmunitario Innato", estas presentan la capacidad citotóxica, que implica la provocación de "apoptosis celular", mediante una interfase llamada "Sinapsis inmunológica", en una manera muy específica en su función letal, pues son capaces de destruir a la célula objetivo sin afectar a las células vecinas, que no están infectadas.
Colangiocitos o Células ductales, células epiteliales que forman la pared de los pequeños ductos por los que circula la bilis, el tracto biliar intra y extrahepático y se distribuyen en una red tridimensional de ductos interconectados. Su función principal es la de sensar y modificar la composición de la bilis proveniente de los cálculos biliares.
De todo lo anterior se desprende la importancia que tiene el de mantener a este órgano en un estado adecuado, desde hace mucho tiempo con el objetivo de comprobar la salud general del hígado se han encontrado pruebas para lograrlo, también conocidas como panel de función hepática, y que es el análisis de la sangre, en el que se miden diferentes: enzimas, proteínas y sustancias producidas por el hígado.
Dicho examen sanguíneo mide los niveles de: proteínas totales, albúmina, bilirrubina y enzimas hepáticas; Tal existencia de niveles altos o bajos podría significar que hay un daño o enfermedad del órgano. Su establecimiento se debe al interés de diagnosticar en un tiempo tiempo adecuado, en la medida de lo posible de forma preventiva, algunas alteraciones que producirán enfermedades, cuyos síntomas no aparecen en etapas tempranas. Algunas de ellas pueden ser: la presencia de cáncer hepático, infecciones del hígado, como la hepatitis; o bien, supervisar el avance de hepatitis, ya sea de origen viral o alcohólica, y también para determinar si el tratamiento es o no efectivo, medir la gravedad de una enfermedad ya declarada, en especial la cicatrización del hígado (cirrosis); o bien supervisar los posibles efectos secundarios de los medicamentos.
Proteínas
Albumina: principal proteína producida por el hígado. Su función es la de combatir infecciones. Su concentración varía cuando hay alteraciones hepáticas, renales o cuando disminuye su producción o aumenta su destrucción.
Proteínas totales: con esta prueba se miden tanto la albúmina como el resto de proteínas plasmáticas o sanguíneas, entre las que se incluyen los anticuerpos (inmunoglobulinas) que se producen para combatir las infecciones. (1)
Bilirrubina: pigmento amarillo-anaranjado, que es un producto de desecho, producido principalmente durante la destrucción del grupo "hemo" (que es el grupo prostético de las hemoproteínas, que son las proteínas que se encargan de transportar y almacenar oxígeno, movilizar electrones y realizar reacciones de óxido-reducción). Este grupo forma parte de la hemoglobina de los glóbulos rojos de la sangre, que por la presencia del átomo de hierro (FE++) le confieren su color rojo característico. El hígado es el órgano encargado de degradar la bilirrubina para su posterior eliminación.
Enzimas hepáticas:
Alanina aminotransferasa (ALT): se una enzima localizada principalmente en el hígado, ayuda a convertir las proteínas en energía para las células hepáticas, es el mejor medio para detectar la presencia de una hepatitis. Si el hígado se encuentra dañado se libera (ALT) al torrente sanguíneo y aumentan sus niveles.
Fosfatasa alcalina (FA) o (ALP): enzima relacionada con los conductos biliares pero asociada también a los huesos, intestino y placenta de las mujeres durante el embarazo. No obstante, sus concentraciones más elevadas se observan en las células óseas y hepáticas; es importante para descomponer las proteínas. Si los niveles de (ALP) son más altos de lo normal, es posible que el hígado presente alguna enfermedad o daño, como una vía biliar obstruida o ciertas enfermedades óseas.
Aspartato aminotransferasa (AST): enzima localizada en el hígado pero también en otros tejidos, como el corazón y diversos músculos del organismo, ayuda a metabolizar los aminoácidos. Al igual que la (ALT), la (AST) normalmente está presente en la sangre en niveles bajos, el incremento en sus niveles puede indicar daño o enfermedad del hígado o daño muscular.
Pruebas Adicionales:
Gamma-glutamil transferasa (CGT): enzima hallada principalmente en las células del hígado, constituye ser un marcador muy sensible para enfermedad hepática, pero, lamentablemente no es específico, en consecuencia de que no permite diferenciar entre las distintas causas de enfermedad hepática. Su evaluación no se recomienda de forma rutinaria, pero puede utilizarse en conjunto con la (PA) para determinar si el origen de un aumento de (PA) se debe a una alteración en el hígado o en el hueso. En los casos de alcoholismo se pueden encontrar concentraciones muy elevadas de esta enzima.
Lactato deshidrogenasa (LDH): enzima que se libera a la sangre cuando existe una lesión celular. Se encuentra en una gran variedad de células del organismo.
Tiempo de protombina (TP): el hígado produce algunos de los factores de coagulación de la sangre, por lo que un tiempo de protrombina alterado puede indicar la existencia de un daño hepático.
Alfa fetoproteína (AFP): está relacionada con la regeneración y proliferación de las células del hígado, y en ocasiones se produce por la presencia de tumores como el carcinoma hepatocelular.
Autoanticuerpos (2): al detectar su existencia Es posible asociarles con la presencia de hepatitis autoinmune o de cirrosis biliar primaria.
(1) La albúmina sérica representa el 55% de las proteínas de la sangre, contribuye de manera importante a mantener la presión oncótica, que es una forma de presión osmótica debida a la diferencia de concentración de proteínas plasmáticas que existe entre el plasma sanguíneo y el líquido intersticial, del plasma y ayuda, como transportista, a llevar lípidos y hormonas esteroides. Por su parte, las globulinas constituyen el 38% de las proteínas de la sangre y transportan iones, hormonas y lípidos que ayudan a la función inmunológica. El fibrinógeno comprende el 6% de las proteínas de la sangre; la conversión de fibrinógeno en fibrina insoluble es esencial para la coagulación de la sangre. El resto de las proteínas plasmáticas representa el 1%, y son proteínas reguladoras, como enzimas, proenzimas y hormonas. Todas las proteínas de la sangre se sintetizan en el hígado, excepto las globulinas gamma.
Las inmunoglobulinas (anticuerpos) son proteínas de importancia vital que circulan en el torrente sanguíneo y realizan una amplia variedad de funciones. Influyen notablemente sobre el equilibrio de nuestro sistema inmunitario. El tipo predominante de anticuerpo en la sangre humana es la inmunoglobulina "G" (IgG).
Inmunoglobulinas: Inmunoglobulina "A" (IgA) aparecen fundamentalmente en secreciones (saliva, lágrimas, secreción intestinal, etc.), recubriendo mucosas expuestas al ataque de agentes patógenos externos, Inmunoglobulina "G" (IgG), Inmunoglobulina "M" (IgM) estas dos se detectan principalmente en el plasma sanguíneo y en el líquido intersticial, Inmunoglobulina "E" (IgE) estos anticuerpos que, si bien inicialmente se liberan al plasma por las células plasmáticas, son integrados en la membrana de otras células (mastocitos), participando en las reacciones de hipersensibilidad e Inmunoglobulina "D" (IgD) asociada a la membrana de los linfocitos B. Su función primaria de las es la de servir como detectores de antígenos para las células B, por loo que se le localiza en el plasma.
(2) Los anticuerpos antinucleares (ANA): son un grupo de autoanticuerpos producidos por el sistema inmunitario, cuando no consigue distinguirse adecuadamente entre las estructuras propias y ajenas. Los ANA atacan a las estructuras del cuerpo, causando signos y síntomas como inflamación de órganos y tejidos, fatiga y dolores musculares y articulares. Los ANA van dirigidos específicamente contra sustancias del núcleo celular, y de ahí su nombre. No suelen afectar a células vivas porque no pueden llegar a su núcleo. Sin embargo, pueden dañar los tejidos al reaccionar con componentes nucleares que han sido liberados por las células muertas o dañadas. La prueba de los ANA permite diagnosticar enfermedades autoinmunes y descartar otros procesos que tengan signos y síntomas similares. Por ejemplo si se padece lupus eritematoso sistémico (LES) anticuerpos están presentes en casi todos los pacientes con, y en proporción variable en pacientes con otras enfermedades autoinmunes. Además, es posible que aparezcan en bajas concentraciones en muchas otras enfermedades, o incluso en personas sanas. Los anticuerpos antimúsculo liso (SMA): son proteínas producidas por el sistema inmune del organismo, que van dirigidas contra una proteína propia, la "actina". La cual se encuentra en el músculo liso y en otros tejidos, especialmente en el hígado. Los anticuerpos de tipo 1 microsomales de hígado y riñón (anti-LKM-1): son proteínas producidas por el sistema inmunitario dirigidas contra un conjunto de enzimas del organismo conocido como citocromo P450 2D6 (CYP2D6), que se encuentra principalmente en las células hepáticas. El desarrollo de estos anticuerpos se asocia a "hepatitis autoinmune de tipo 2".
La "alfa-fetoproteína" (AFP) es una proteína que normalmente sólo se produce durante el desarrollo fetal. Si aparecen niveles elevados de (AFP) en el líquido amniótico, puede ser una indicación de un defecto en el desarrollo del feto. Al aparecer en la vida adulta, puede servir como un marcador tumoral.
En la cirrosis el hígado se endurece y se vuelve fibrótico, como tejido cicatrizado. Esto se debe a la activación de células llamadas fibroblastos. El nuevo trabajo explica cómo entran en juego: cuando las células predominantes del hígado, hepatocitos, no producen una proteína llamada MCRS1, los ácidos biliares (productos del hígado y componentes de la bilis) se acumulan en el órgano y activan los fibroblastos, que acaban produciendo la fibrosis.
El Grupo de Factores de Crecimiento, Nutrientes y Cáncer del Centro Nacional de Investigaciones Oncológicas (CNIO), liderado por el doctor Nabil Djouder, creó el primer ratón genéticamente modificado que desarrolla cirrosis hepática equiparable a la humana, e identificó los mecanismos moleculares de esta enfermedad.
“Conocer esos mecanismos moleculares ayudará a entender cómo la cirrosis progresa a cáncer de hígado”, señaló Djouder, cuyo trabajo se publicó en la revista "Journal of Hepatology".
En la gráfica, un órgano enfermo en el que distintos tipos de células han sido marcadas con fluoróforos que se distinguen con los colores blanco, verde y rojo. Foto Nabil Djouder/ CNIO.
El primer modelo animal que recapitula la cirrosis hepática humana se obtuvo de forma no buscada. El Grupo de Factores de Crecimiento, Nutrientes y Cáncer estudia desde hace casi una década la proteína microesférula 1 (MCRS1).
Hace varios años descubrió su relación con el metabolismo y con varios tipos de cáncer. Dado que el principal órgano responsable del metabolismo es el hígado, quisieron también analizar el papel de MCRS1 en las células hepáticas.
Esta proteína es codificada por el gen MCRS1, que corresponde a la carga del cromosoma 12, se estima que este cromosoma posee alrededor de 133 millones de "pares de bases", que representan entre el 5 y el 8% del ácido desoxirribonucleico (ADN) total de la célula humana, y que alberga una cantidad estimada de entre un mil doscientos y un mil seiscientos genes.
Amanda Garrido y Eunjeong Kim, quienes son las primeras firmantes del trabajo, crearon un ratón modificado genéticamente de forma que sus hepatocitos no expresaran MCRS1, y observaron que desarrollaba alteraciones equivalentes a la cirrosis hepática humana.
Destacó Djouder: “Fue una sorpresa que abrió una oportunidad para estudiar los mecanismos moleculares de la cirrosis y su progresión a cáncer, e intentar así revertir la enfermedad. Y se complemento lo anterior con un señalamiento realizado por Garrido: "En efecto, entender por qué la falta de MCRS1 en los hepatocitos genera cirrosis ha supuesto desvelar un proceso hasta ahora desconocido como origen de la enfermedad, y abre la puerta al desarrollo de nuevas estrategias farmacológicas”.
Hasta ahora se sabía que la fibrosis del hígado implicaba la transformación de las células estrelladas hepáticas en fibroblastos, que sintetizan la sustancia que forma el tejido cicatrizado o la fibrosis. Sin embargo, se desconocían los mecanismos desencadenantes de ese cambio y la consiguiente activación de los fibroblastos.
La falta de MCRS1 en los hepatocitos altera el flujo de los ácidos biliares, los cuales activan en los fibroblastos un "receptor molecular" llamado FXR, que actúa como el detonante que pone en marcha el proceso de la cirrosis.
Ha precisado Djouder: “Esta cadena de eventos es central y universal en el desarrollo de la cirrosis hepática. Actuar sobre esta vía tendría implicaciones importantes para el tratamiento de la enfermedad”.
Además, esto revela una función desconocida de MCRS1 en la regulación de la expresión de los genes en los hepatocitos y en el funcionamiento normal del hígado.
Sobre el receptor FXR actúa un fármaco contra varias enfermedades del hígado en ensayo en Estados Unidos, el ácido biliar semisintético Ocaliva. Sin embargo, datos clínicos recientes han alertado en torno a posibles efectos adversos: su uso provocó fibrosis grave y daño hepático fulminante en algunos pacientes.
Se conocen cuatro clases de cáncer primario de hígado: hepatocarcinoma, colangiocarcinoma, angiosarcoma y hepatoblastoma. El 98% de los casos de cáncer primario de hígado son de origen epitelial; de éstos, 85% corresponden a carcinoma hepatocelular (CHC), con más de cuatrocientos cincuenta mil casos anuales a nivel mundial. Su incidencia y prevalencia varían según área geográfica, género, edad y factores de riesgo.
Este tipo de afección presenta una tasa de alta mortalidad; el (CHC) representa alrededor del noventa por ciento del total de casos de cáncer hepático en el mundo, se cuenta con la estadística de nos dice que el 75% del total la afectación se presenta entre los varones y que la edad de detección es superior a los cuarenta y cinco años.
Más del ochenta por ciento de los casos de CHC del mundo corresponden a población asiática y africana, y los países con las tasas de incidencia mas altas (20-500) son Japón, China, Corea, Taiwán, Mozambique y Nigeria; mientras que entre las naciones con tasas de incidencia intermedia (10-19) se cuentan los países del mediterráneo y Brasil, y, con tasas de incidencia bajas, se encuentra el norte de Europa, Australia, Nueva Zelanda, y la mayor parte de América.Por ejemplo en Colombia la tasa de incidencia es de 2.2 por cada cien mil habitantes para los hombres y 2.0 para las mujeres.
Como sucede con el cáncer primario de hígado, la incidencia de CHC es dos a tres veces mayor en hombres que en mujeres, pero en las zonas de alta incidencia puede ser hasta ocho veces mayor en población masculina. Sin embargo, las cifras dicen que esta regla no parece cumplirse en los países de baja incidencia, pues según se deduce de algunos estudios realizados en Sudamérica, llevada a cabo en países como: Colombia, Ecuador y Perú, se registró una relación hombre-mujer cercana al 1:1.
Según un estudio realizado por la Organización Mundial de la Salud (OMS), las prevalencias de la infección por el virus de la hepatitis B (VHB) y de la infección por el virus de la hepatitis C (VHC) en pacientes con CHC tienen una distribución diferente de acuerdo con las regiones del mundo. Es así como el CHC asociado al VHB tiene mayor prevalencia en África, gran parte de América y China, mientras que el CHC asociado al VHC tiene mayor prevalencia en Japón, Estados Unidos, México y gran parte de Europa.
Este estudio también mostró de manera global que en el setenta y ocho por ciento de los pacientes con CHC la causa fue atribuible a VHB (53%) y a VHC (25%). La distribución agrupada por edades, de los casos está relacionada principalmente con la edad de adquisición de la infección por VHB o VHC. Según lo descrito en la literatura el riesgo de desarrollar CHC aumenta de dos a tres veces por cada década de vida. En países de baja incidencia el mayor número de casos se reportan entre la quinta y la sexta década de vida, mientras que en regiones con alta incidencia los casos se presentan entre la tercera y la cuarta. Esta diferencia es debida a que la principal ruta de transmisión de la infección por el VHB es vertical en las regiones de alta incidencia, lo que incrementa el riesgo de desarrollar infección crónica y CHC en edades mas tempranas; a su vez, el VHC se adquiere principalmente en la edad adulta a través de transfusiones e inyecciones, y no es frecuente el contagio a edades tempranas, lo que podría explicar que en regiones donde la infección por este virus es más frecuente, el cáncer se desarrolle más tardíamente.
El CHC puede ser asintomático por varios años, o presentarse con síntomas confusos que podrían atribuirse a las patologías de base que usualmente lo acompañan, lo que hace que su detección se haga generalmente en estadios avanzados. Desde el momento en que la enfermedad se manifiesta clínicamente, la progresión es rápida; es así como la mayoría de los pacientes sin tratamiento fallecen tres a seis meses después del diagnóstico; cuando es detectado en etapas iniciales la supervivencia puede ser de uno a dos años luego de la resección quirúrgica del tumor, en los casos en los que sea posible realizar este procedimiento. El trasplante hepático ofrece supervivencia de 70-75% a cinco años en pacientes con estadificación temprana del tumor, según la clasificación de Milán.
También se estima que anualmente se detectan más de ochocientos cincuenta mil casos; siendo el sexto tipo de cáncer más frecuente, se calcula que al año mueren ochocientas mil personas por esta causa y se observa un incremento entre los que lo padecen, debido a que se ha incrementado la incidencia del "hígado graso no alcohólico" entre la población.
En México, las estadísticas indican que es la segunda causa de muerte, según datos presentados por la Secretaria de Salud, pues hay mas de cinco mil decesos anuales, y las cifras de detección indican ocho mil casos anuales. Se indica que los cinco tipos de cáncer que otorgan mayor mortalidad, números absolutos, en el país son: pulmonar, hepático, colorrectal, gástrico y mamario, en orden descendente.
Según las cifras dadas a conocer en un boletín de prensa por el Instituto Nacional de Estadística y Geografía (INEGI), el día 4 de febrero pasado, con motivo del día mundial contra el cáncer:
Durante el año 2020 se registraron 1'086,743 defunciones en México, de las cuales el ocho por ciento fueron por tumores malignos (90,603 casos). La tasa de defunciones por esta causa aumentó durante la última década, al pasar de 6.18 defunciones por cada 10 mil personas en 2010 a 7.17 por cada 10 mil personas en 2020.
Tasa de Defunciones por tumores malignos (por año de registro)
Defunciones por cada diez mil habitantes para cada año de registro
Año Tasa
2010 6.18
2011 6.18
2012 6.26
2013 6.35
2014 6.43
2015 6.55
2016 6.72
2017 6.78
2018 6.84
2019 7.01
2020 7.17
Para el 2020, se entregó la siguiente información a mayor detalle:
Tasa de Defunciones por Tumores Malignos
por Grupos Decenales de edad y Sexo.
defunciones por cada 10 mil habitantes
Grupo de edad Total Hombres Mujeres
Total 7.17 7.21 7.13
de 0 a 9 años 0.41 0.46. 0.35
de 10 a 19 años 0.61 0.72 0.51
de 20 a 29 años 1.02 1.22 0.82
de 30 a 39 años 1.93 1.64 2.19
de 40 a 49 años 4.98 3.61 6.24
de 50 a 59 años 11.29 9.57 12.83
de 60 a 69 años 24.52 25.41 23.73
de 70 a 79 años 48.17 55.97 41.35
de 80 y más 79.84 104.82 60.80
Tasa de Defunciones por causas de tumor Maligno
por Grupos de Edad y Sexo, año 2020.
defunciones por cada 10 mil habitantes

Al analizar las defunciones por grupos de edad y tipo de tumores malignos, destaca que, entre los principales tipos de cáncer que afectaron.
Entre la población infantil de 0 a 14 años son:
Hombres (0.47): leucemia (0.24); tumor maligno de las meninges, del encéfalo y de otras partes del sistema nervioso central (0.08); tumor maligno del hígado y de las vías biliares intrahepáticas (0.02), así como de linfoma no Hodgkin (0.02).
Mujeres (0.37): leucemia (0.19); tumor maligno de las meninges, del encéfalo y de otras partes del sistema nervioso central (0.06); tumor maligno del hígado y de las vías biliares intrahepáticas (0.01), así como de linfoma no Hodgkin (0.01).
Entre los jóvenes de 15 a 29 años son:
Hombres (1.13): leucemia (0.36); tumor maligno de las meninges, del encéfalo y de otras partes del sistema nervioso central (0.06); linfoma no Hodgkin (0.06) y tumor maligno del estómago (0.04).
Mujeres (0.74): leucemia (0.25), tumor maligno del ovario (0.06); tumor maligno del cuello del útero (0.06), así como tumor maligno de las meninges, del encéfalo y de otras partes del sistema nervioso central (0.05).
Entre los adultos de 30 a 59 años son:
Hombres (4.42): tumor maligno del colon, del recto y del ano (0.55), tumor maligno del estómago (0.47), tumores malignos de la tráquea, de los bronquios y del pulmón (0.32), así como leucemia (0.31).
Mujeres (6.46): tumor maligno de la mama (1.56), así como el del cuello del útero (0.86), tumor maligno del ovario (0.54), así como tumor maligno de estómago (0.43).
Entre los adultos mayores de 60 años y más son:
Hombres (45.35): tumor maligno de la próstata (10.89), tumores malignos de la tráquea, de los bronquios y del pulmón (4.79), tumor maligno del colon, del recto y del ano (3.95), así como tumor maligno del hígado y de las vías biliares intrahepáticas (3.81).
Mujeres (34.61): tumor maligno de la mama (4.71), tumor maligno del hígado y de las vías biliares intrahepáticas (3.34), tumor maligno del colon, del recto y del ano (2.82), así como tumor maligno de estómago (2.57) .
De la lectura de la tabla anterior se desprende que el cáncer de el hígado y de las vías biliares intrahepática, es bastante frecuente, pero no es el único, hay otros dos tipos de malignidad que se fomenta entre los mexicanos.
El cáncer de próstata, una de las enfermedades que más afecta a los varones en México, esto es una consecuencia de los tabúes y estigmas vigentes entre la población, pues el setenta por ciento de los casos se detectan en etapas avanzadas; cuidar su vida es lo que está de por medio, enfatizó el Director General del Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado (ISSSTE), Luis Antonio Ramírez Pineda, quien declaró lo anterior en una entrevista realizada el primer día de diciembre del 2020. La prevención es el camino, y pidió a trabajadores, pensionados y derechohabientes varones tomen en sus manos el cuidado de su salud y prevenir el cáncer de próstata, ya que esta enfermedad cuando evoluciona se disemina principalmente en huesos y causa múltiples complicaciones que afectan drásticamente la calidad de vida de los pacientes.
Tras afirmar que de acuerdo con el Instituto Nacional de Salud Pública (INSP) el cáncer de próstata causa 9.8 muertes por cada 100 mil habitantes, es decir que cobra alrededor de siete mil vidas anuales en México, el titular del Instituto refirió que estadísticas institucionales indican que los hombres derechohabientes van con menor frecuencia a las unidades médicas. Al registrarse la pérdida de unas siete mil vidas anuales, se mantiene el exhortó a este sector de la población a acudir anualmente -a partir de los cincuenta años- a las unidades médicas a realizarse un "tamizaje", mediante pruebas de antígeno prostático y tacto rectal, pueden hacer la diferencia entre curarse o ser enfermo de por vida, para detectar la enfermedad en etapas tempranas, cuando no hay síntomas y es curable. Es recomendable iniciar el "tamizaje" anual a los 45 años en hombres con antecedentes de cáncer de próstata en padre o hermanos a edades tempranas. Se puntualiza que el factor incluido en la carga genética también es un punto a considerar.
El cáncer de mama no tiene una causa única; se han identificado una serie de factores que contribuyen en su aparición y desarrollo; por ejemplo la edad, conforme las personas envejecen aumenta el riesgo de padecerlo; el inicio temprano de la menstruación, antes de los 12 años, e inicio tardío de la menopausia, después de los 55 años; antecedentes de cáncer de seno o de ovario; la obesidad y el sobrepeso; el tabaquismo y la ingesta de alcohol; algunas terapias de reemplazo hormonal y ciertos anticonceptivos orales; así como mutaciones genéticas heredadas en los genes BRCA1, BRCA2.
Breast cancer 1, «Cáncer de mama 1» (BRCA1) es un gen supresor de tumores humano, queregula el ciclo celular y evita la proliferación incontrolada. La proteína BRCA1, producto de este gen, forma parte del sistema de detección y reparación de los daños del ADN,está situado en el brazo largo (q) del cromosoma 17, en la posición 21. Diversas mutaciones de este gen están implicadas en algunos tipos de cáncer, especialmente el de mama. En las mujeres portadoras de mutaciones en el gen BRCA1, el riesgo acumulado hasta los 70 años se estima entre 51 y 95% para cáncer de mama y entre 22 y 66% para cáncer de ovario.
Estructura tridimensional de la proteína Breast Cancer 2 Susceptibility. Wikipedia.
Breast Cancer Type 2 susceptibility protein (BRCA2) está localizado en el brazo largo (q) del cromosoma 13, en la posición 12.3 (13q12.3). Las mujeres que presentas mutaciones tienen un riesgo acumulado hasta los 70 años de entre 33 y 95% para cáncer de mama y entre 4 y 47% para cáncer de ovario.
En el mundo cada año se registran 685 mil defunciones por cáncer de mama, siendo entre los tumores malignos, la principal causa de muerte en las mujeres.
Incidencia de cáncer de mama en la población mexicana de 20 años y más por sexo 2010 a 2019
(Por cada 100 mil personas de 20 años y más de cada sexo)
Nota: Se utilizó la Clasificación Estadística Internacional de Enfermedades y Problemas Relacionados con la Salud (CIE-10), código C50. Excluye casos con edad no especificada.
Fuentes: SALUD, Dirección General de Epidemiología (DGE). (2021). Anuarios de Morbilidad 1984-2019. CONAPO (2018). Proyecciones de la Población de México y de las Entidades Federativas, 2016-2050.
En México durante 2019 se registraron 15 mil 286 nuevos casos de cáncer de mama en la población de 20 años y más. De estos, 167 corresponden a hombres y 15 mil 119 a mujeres. La tasa de incidencia de tumor maligno de mama a nivel nacional es de 18.55 casos nuevos por cada 100 mil habitantes de 20 años y más.
 Fuente: elaboración propia con base en el comunicado del INEGI: “Estadísticas a propósito del Día Mundial de la Lucha contra el Cáncer de Mama”.
Fuente: elaboración propia con base en el comunicado del INEGI: “Estadísticas a propósito del Día Mundial de la Lucha contra el Cáncer de Mama”.
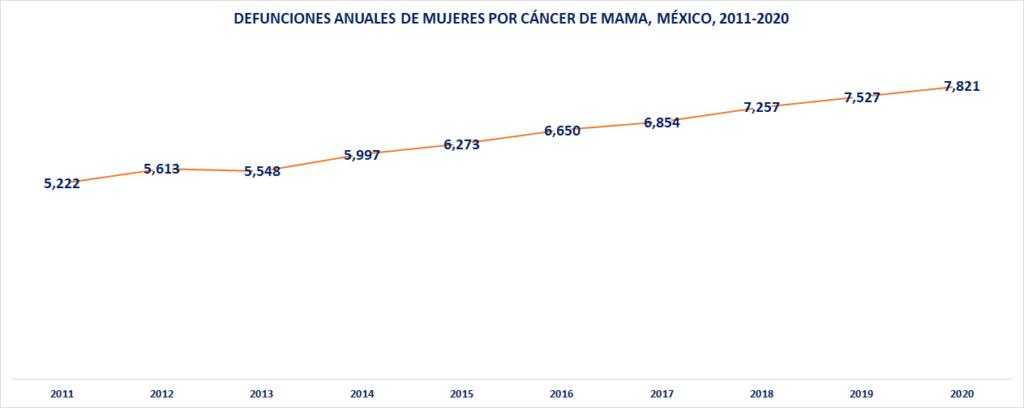
Fuente: elaboración propia con base en las estadísticas de mortalidad de INEGI:
En 2020, según las cifras preliminares de ese año, fallecieron 97 mil 323 personas por tumores malignos. De estos, 7 mil 880 fueron por tumores malignos de mama, 7 mil 821 mujeres y 59 hombres, el total equivale a el ocho por ciento de este total; entre la población femenina esto equivale a 17% del total de defunciones por tumores malignos y la ubica en primer lugar de esta clasificación.
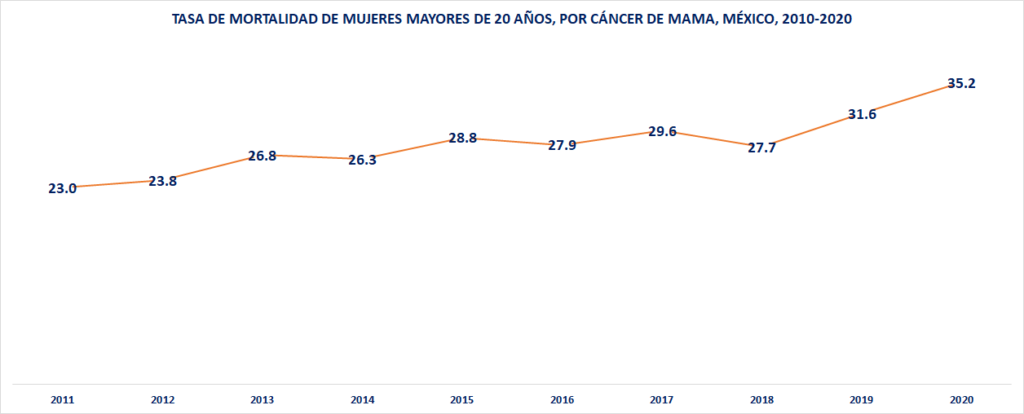
Tasa de mortalidad por cáncer de mama en mujeres de 20 años y más por grupo de edad 2020
(Defunciones por cada 100 mil mujeres)
Nota: Se utilizó la Clasificación Estadística Internacional de Enfermedades y Problemas Relacionados con la Salud (CIE-10), código C50 (Tumor maligno de la mama). Se excluyó la defunción de una mujer menor de 20 años.
Fuentes: INEGI. Estadísticas de mortalidad 2020. Datos preliminares. Consulta interactiva de datos. SNIEG. Información de Interés Nacional.
CONAPO (2018). Proyecciones de la Población de México y de las Entidades Federativas, 2016-2050.
La tasa más alta de defunciones de mujeres por cáncer de mama se registra en el grupo de edad de 60 años o más (49.08 por cada 100 mil mujeres de este grupo de edad, 4.71 por diez mil habitantes ), pero también alcanza números elevados en el rango de los 30 a los 59 años (1.56 por diez mila habitantes) y es la primera causa en dicho rango. Ahora que si se toman las cifras preliminares, nos acercamos a un desglose más preciso; por edad al fallecimiento son pocas las mujeres jóvenes de 20 a 29 años que mueren por cáncer de mama (0.64 defunciones por cada 100 mil mujeres de este grupo de edad), seguidas de las de 30 a 44 con una tasa de 7.09 defunciones por cada 100 mil. Las tasas más altas se registran en los grupos de 45 a 59 años y de 60 años o más (26.79 y 49.08 defunciones de mujeres por cada 100 mil mujeres, respectivamente); es decir, este padecimiento conforme se incrementa la edad, propicia más mortalidad.
Al igual que en el caso del cáncer de próstata, en el de seno, también existen prejuicios, como el machismo, la vergüenza o priorizan la atención de la familia y en muchos casos la detección es tardía, en los casos positivos solo un veinte por ciento se da en etapa temprana, un cuarenta por ciento en intermedia y una cifra similar en estado avanzado. La expectativa de vida en la actualidad para un padecimiento de este tipo es muy alta, pero se requiere una detección oportuna.
Esta vista panorámica sobre el cáncer, nos lleva a entender la causa de las continuas y profundas investigaciones que sobre la enfermedad realizan grupos de científicos, investigadores, biólogos, etcétera, a lo largo y ancho del mundo. Los avances que se logran, dan nuevas esperanzas y propician que no se deje de lado el trabajo colectivo que cientos o quizás miles de seres humanos llevan a cabo. La Machincuepa Cuántica se mantiene atenta sobre el tema.
 Fuente: elaboración propia con base en el comunicado del INEGI: “Estadísticas a propósito del Día Mundial de la Lucha contra el Cáncer de Mama”.
Fuente: elaboración propia con base en el comunicado del INEGI: “Estadísticas a propósito del Día Mundial de la Lucha contra el Cáncer de Mama”.










Comentarios
Publicar un comentario